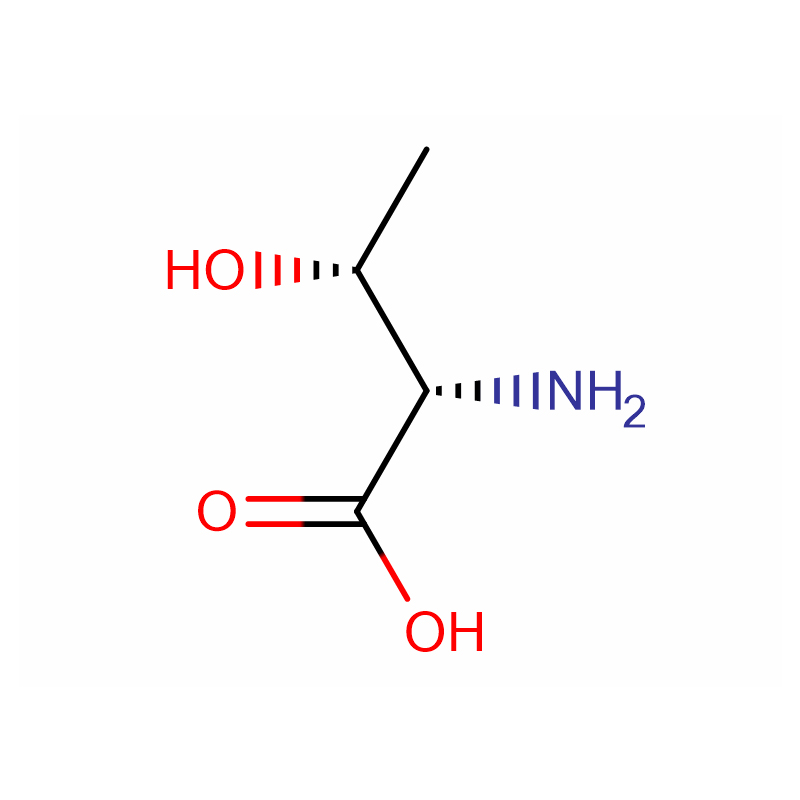
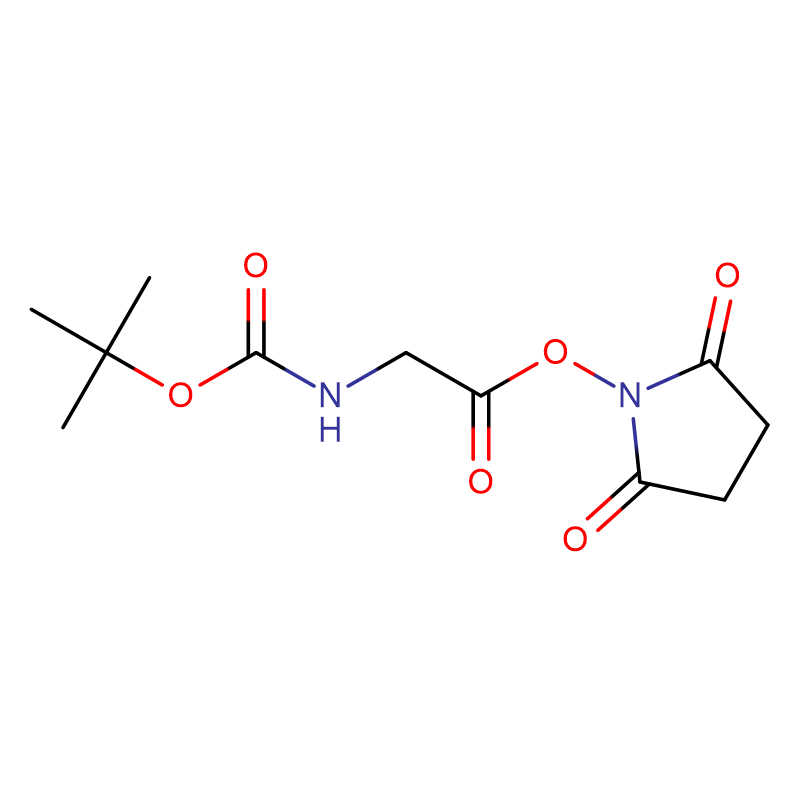
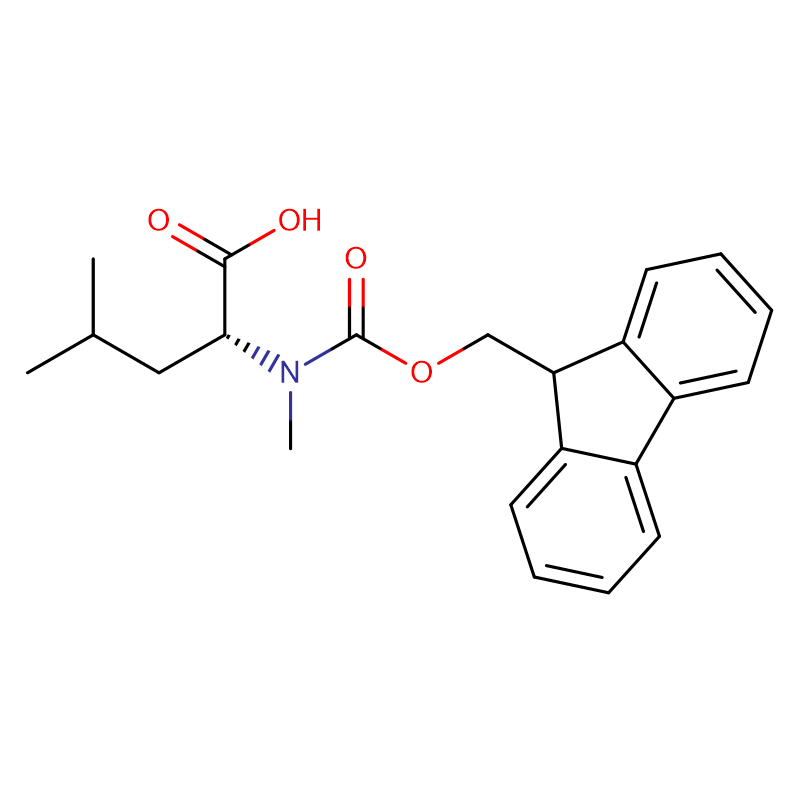
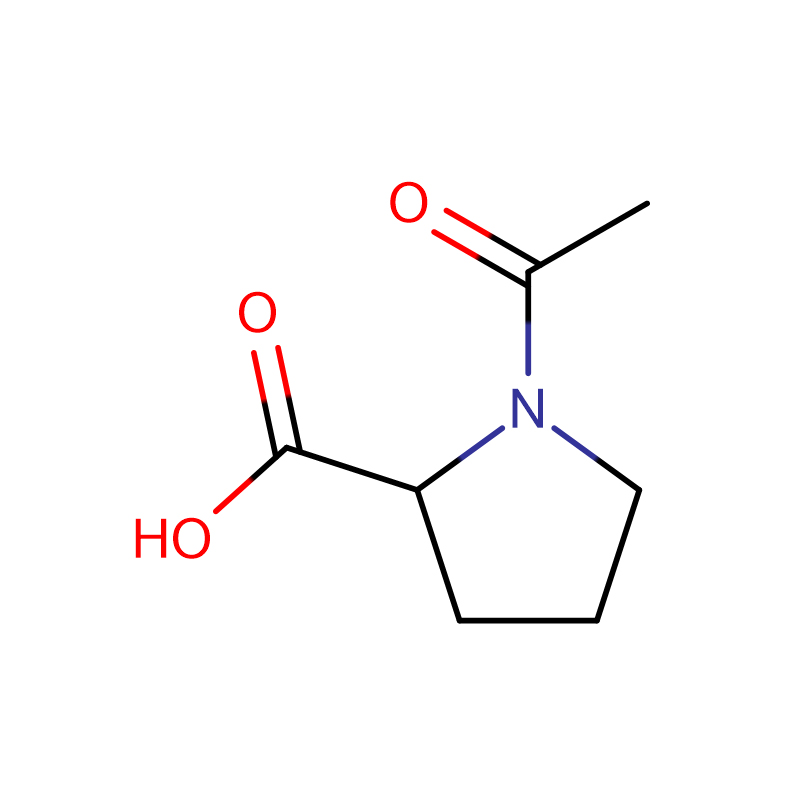
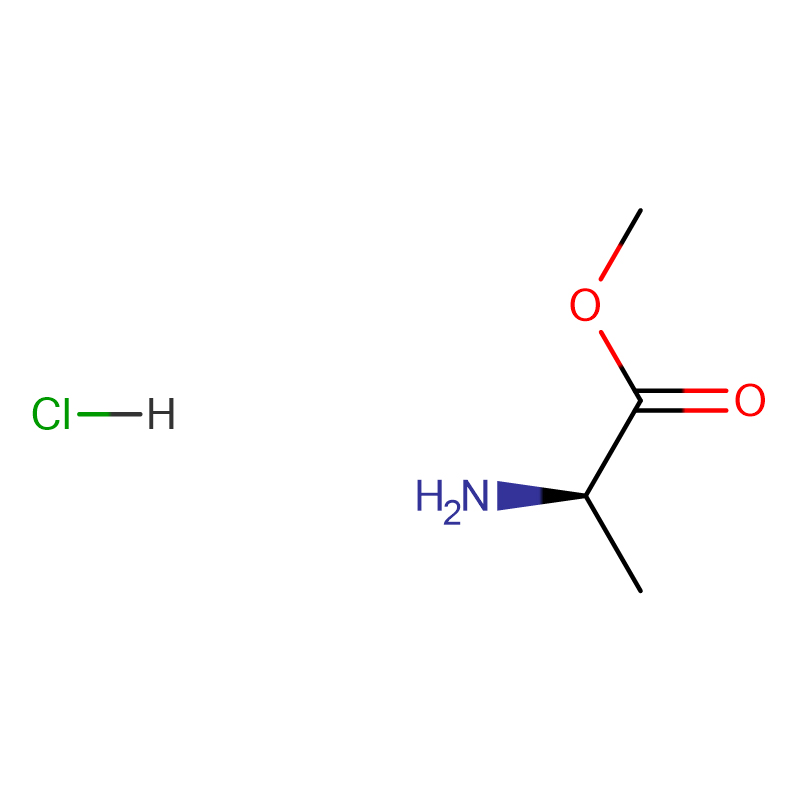
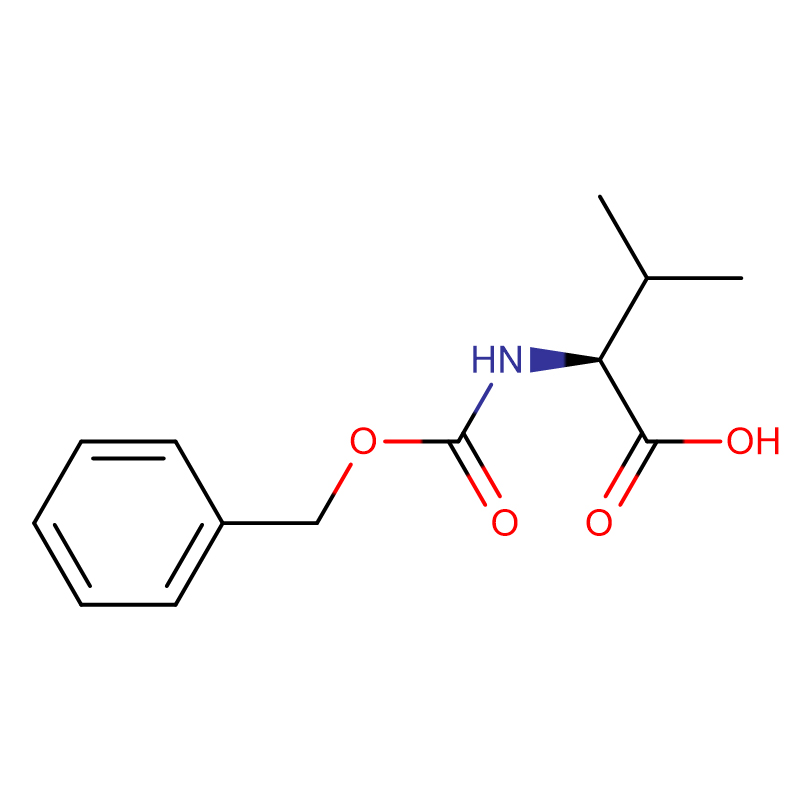
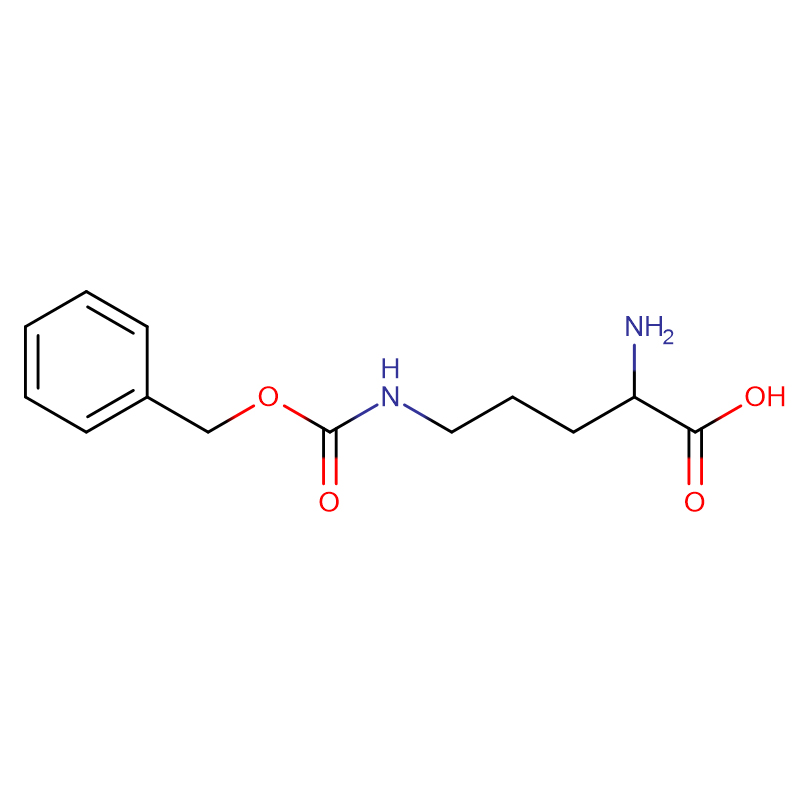
(2S,3R)-2-Amino-3-hydroxybuttersäure Cas: 72-19-5 99 % Weißes kristallines Pulver
| Katalognummer | XD90285 |
| Produktname | (2S,3R)-2-Amino-3-hydroxybuttersäure |
| CAS | 72-19-5 |
| Molekularformel | C4H9NO3 |
| Molekulargewicht | 119.11916 |
| Speicherdetails | Umgebungs |
| Harmonisierter Tarifkodex | 29225000 |
Produktspezifikation
| Test | 99 - 101 % |
| Aussehen | weißes kristallines Pulver |
| Bestimmte Rotation | -27,5 bis -29,0 |
| Schwermetalle | 10 ppm max. |
| AS | Maximal 10 ppm |
| pH | 5,2 - 6,5 |
| SO4 | <0,020 % |
| Fe | Maximal 10 ppm |
| Trocknungsverlust | <0,20 % |
| Glührückstand | <0,10 % |
| Transmission | NLT 98 % |
| Cl | <0,02 % |
| Ammoniumsalz | <0,02 % |
Serin/Threonin-Proteinphosphatasen wurden in vielen pathogenen Bakterien als essentielle Enzyme beschrieben, die an phosphorylierungsabhängigen Signaltransduktionswegen beteiligt sind und häufig mit der Virulenz dieser Organismen in Zusammenhang stehen.Eine Untersuchung des Genoms von Mycoplasma synoviae ergab das Vorhandensein eines Gens (prpC), das für eine mutmaßliche Proteinphosphatase der Proteinphosphatase 2C (PP2C)-Unterfamilie kodiert.Hier berichten wir über eine vollständige biochemische Charakterisierung der M. synoviae-Phosphatase (PrpC) und die besondere Rolle von Metallionen in der Struktur-Funktions-Beziehung dieses Enzyms.Die PrpC-Aminosäuresequenzanalyse ergab, dass alle am zweikernigen Metallzentrum beteiligten Reste und die mutmaßlichen dritten Metallionen-koordinierenden Reste, die in PP2C-Phosphatasen konserviert sind, in PrpC vorhanden sind.PrpC ist ein Monomerprotein, das in der Lage ist, Phosphosubstrate in Abhängigkeit von Mn(2+)-Ionen zu dephosphorylieren.Die Analyse der thermischen Stabilität zeigte die Stabilität des Enzyms bei milden Temperaturen und den Einfluss von Mn(2+)-Ionen auf diese Eigenschaft.Die massenspektrometrische Analyse deutete darauf hin, dass drei Metallionen an PrpC binden, zwei davon mit scheinbar hoher Affinitätskonstante.Eine Mutationsanalyse der mutmaßlichen dritten metallkoordinierenden Reste Asp122 und Arg164 ergab, dass diese Varianten eine schwächere Bindung von Manganionen aufwiesen und dass beide Mutationen die PrpC-Phosphataseaktivität beeinflussten.Diesen Ergebnissen zufolge ist PrpC ein metallabhängiges Proteinphosphatase-Mitglied mit einer verbesserten Stabilität in der Holoform und mit Asp122, das möglicherweise an der dritten Metallbindungsstelle beteiligt ist und für die katalytische Aktivität essentiell ist.