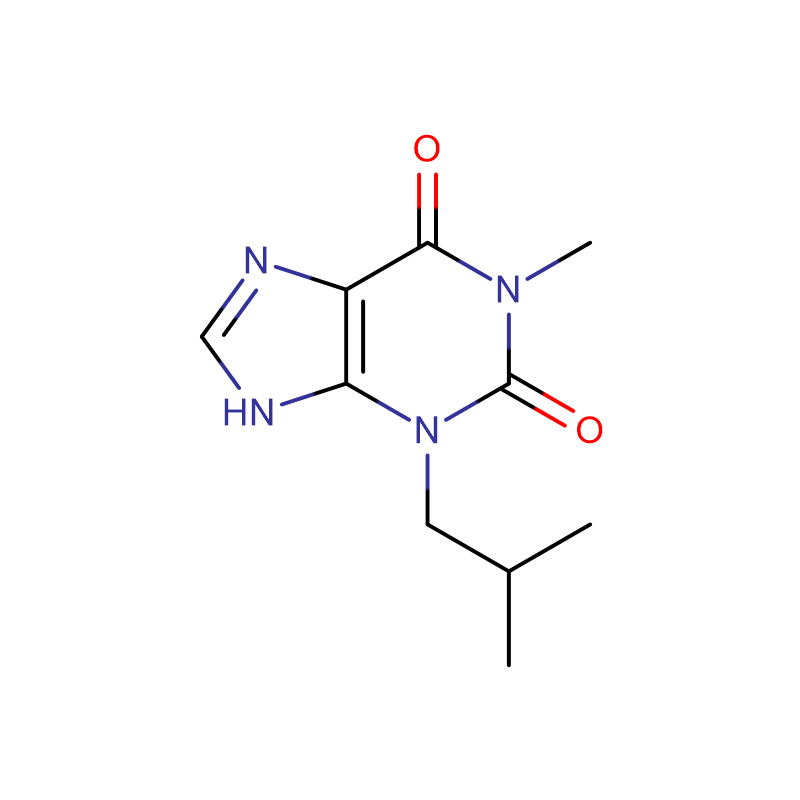
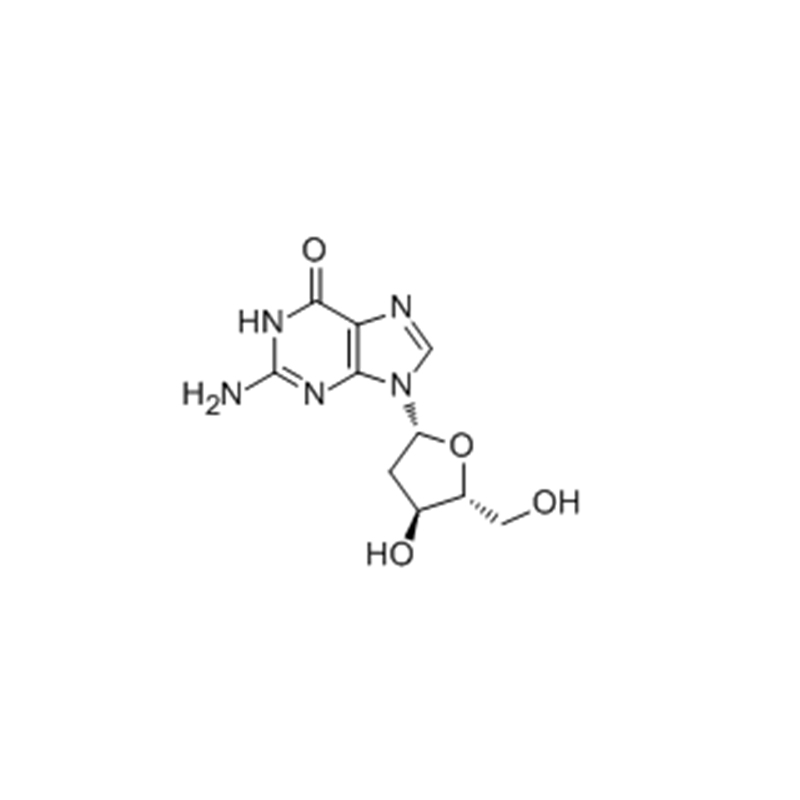
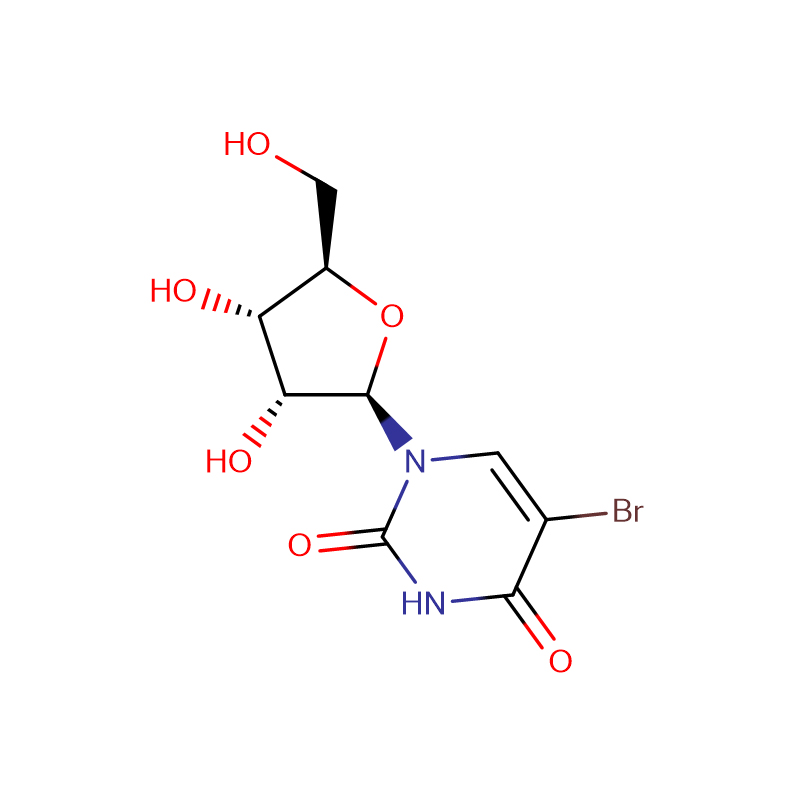
ITP, Inosin-5′-triphosphat-Trinatriumsalz
| Katalognummer | XD90558 |
| Produktname | ITP, Inosin-5'-triphosphat-Trinatriumsalz |
| CAS | 35908-31-7 |
| Molekularformel | C10H12N4Na3O14P3 |
| Molekulargewicht | 574.111 |
| Speicherdetails | Umgebungs |
| Harmonisierter Tarifkodex | 29349990 |
Produktspezifikation
| Aussehen | weißes Puder |
| Test | 99 % |
Infrarotspektroskopie wurde verwendet, um Substrat-Protein-Wechselwirkungen abzubilden: Die Konformationsänderungen der Ca(2+)-ATPase des sarkoplasmatischen Retikulums bei Nukleotidbindung und ATPase-Phosphorylierung wurden mithilfe des Substrats ATP und ATP-Analoga (2'-Desoxy-ATP, 3) überwacht '-Desoxy-ATP und Inosin-5'-triphosphat), die an bestimmten funktionellen Gruppen des Substrats modifiziert wurden.Modifikationen an der 2'-OH-, der 3'-OH- und der Aminogruppe von Adenin verringern das Ausmaß der bindungsinduzierten Konformationsänderung der ATPase, wobei bei den beiden letzteren besonders starke Auswirkungen beobachtet wurden.Dies zeigt die strukturelle Empfindlichkeit des Nukleotid-ATPase-Komplexes gegenüber individuellen Wechselwirkungen zwischen Nukleotid und ATPase.Alle untersuchten Gruppen sind für die Bindung wichtig und die Wechselwirkungen einer bestimmten Ligandengruppe mit der ATPase hängen von den Wechselwirkungen anderer Ligandengruppen ab.Eine Phosphorylierung der ATPase wurde für ITP und 2'-Desoxy-ATP beobachtet, nicht jedoch für 3'-Desoxy-ATP.Es besteht kein direkter Zusammenhang zwischen dem Ausmaß der Konformationsänderung bei der Nukleotidbindung und der Phosphorylierungsrate, was zeigt, dass das volle Ausmaß der ATP-induzierten Konformationsänderung für die Phosphorylierung nicht zwingend erforderlich ist.Wie beim Nukleotid-ATPase-Komplex beobachtet, hängt die Konformation des ersten phosphorylierten ATPase-Zwischenprodukts E1PCa(2) auch vom Nukleotid ab, was darauf hindeutet, dass ATPase-Zustände eine weniger einheitliche Konformation aufweisen als bisher angenommen.