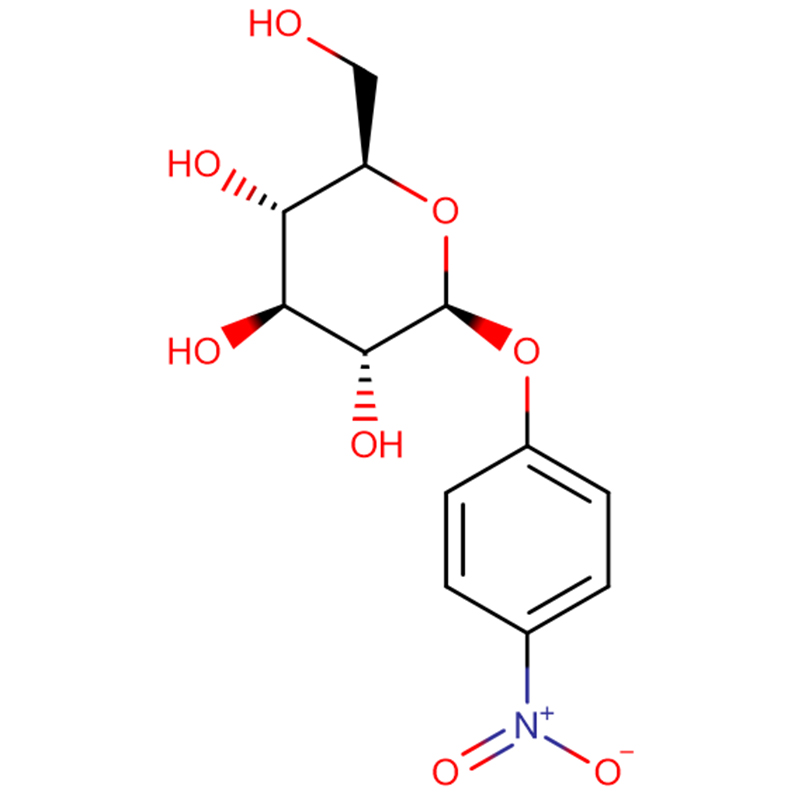
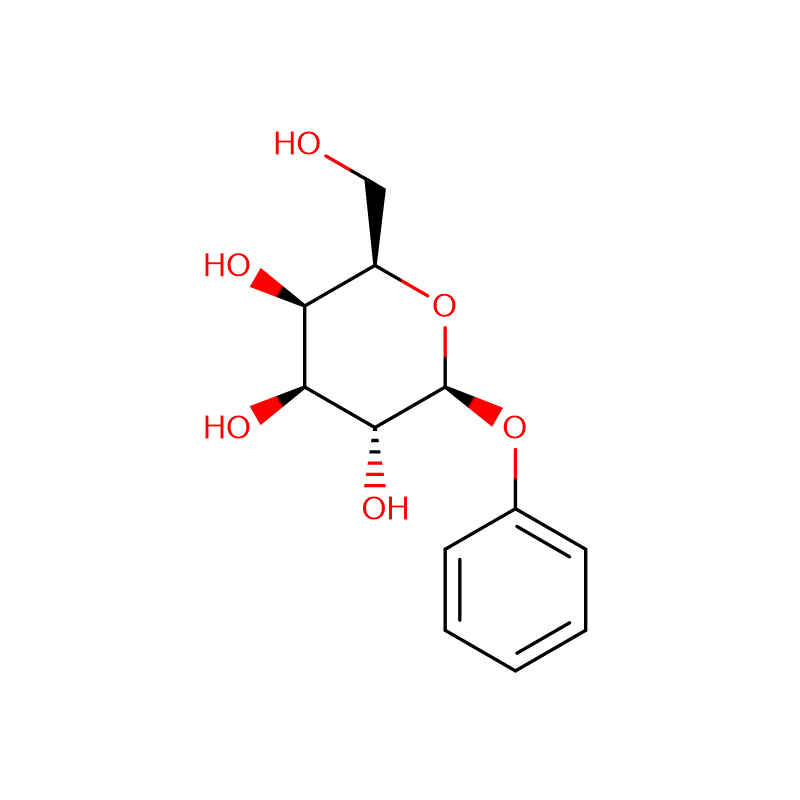
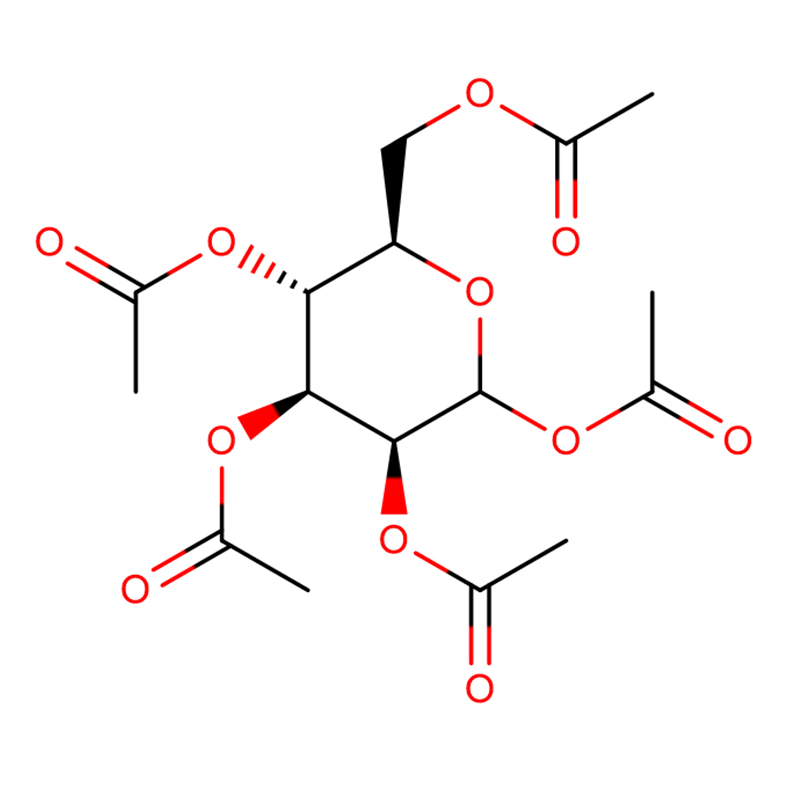
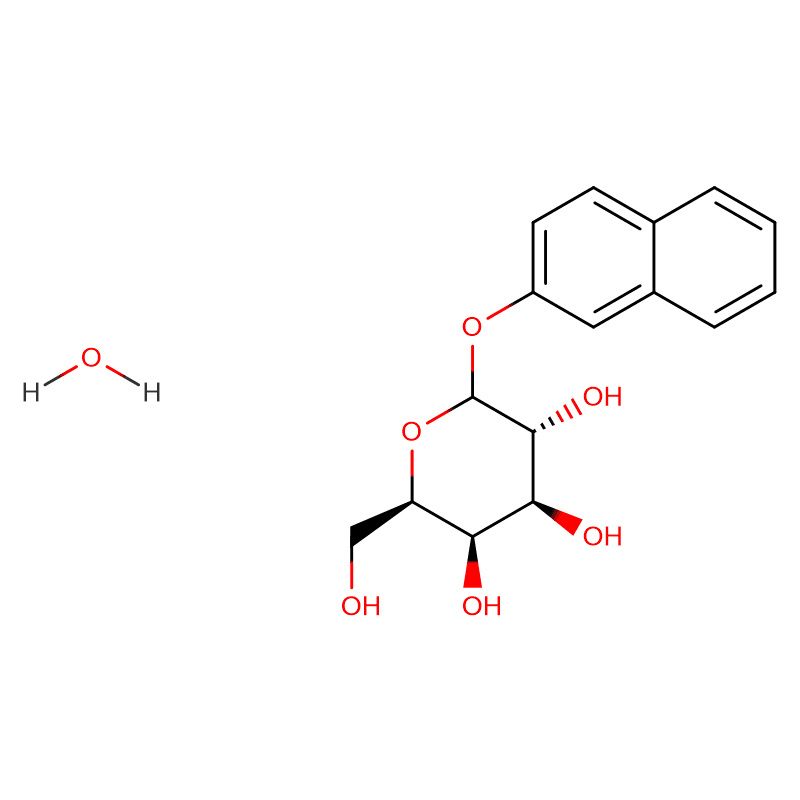
Ein neues β-Glucosidase-Gen, bgl1G5, wurde aus Phialophora sp. kloniert.G5 und erfolgreich in Pichia pastoris exprimiert.Die Sequenzanalyse ergab, dass das Gen aus einem offenen Leserahmen von 1.431 bp besteht, der ein Protein mit 476 Aminosäuren kodiert.Die abgeleitete Aminosäuresequenz von bgl1G5 zeigte eine hohe Identität von 85 % mit einer charakterisierten β-Glucosidase aus Humicola grisea aus der Glycosidhydrolase-Familie 1. Im Vergleich zu anderen Pilzgegenstücken zeigte Bgl1G5 eine ähnlich optimale Aktivität bei pH 6,0 und 50 °C und war stabil bei pH 5,0–9,0.Darüber hinaus zeigte Bgl1G5 eine gute Thermostabilität bei 50 °C (6 h Halbwertszeit) und eine höhere spezifische Aktivität (54,9 U mg–1).Die K m - und V max -Werte für p-Nitrophenyl-β-D-glucopyranosid (pNPG) betrugen 0,33 mM bzw. 103,1 μmol min–1 mg–1.Der Substratspezifitätstest zeigte, dass Bgl1G5 hochaktiv gegen pNPG, schwach gegen p-Nitrophenyl-β-D-Cellobiosid (pNPC) und p-Nitrophenyl-β-D-galactopyranosid (ONPG) war und keine Aktivität gegen Cellobiose aufwies.